Los elementos químicos se clasifican en metales y no metales. Los metales son las sustancias que conducen electricidad, pueden formar láminas o alambres y tienen brillo. Los no metales son todas aquellas sustancias que no conducen electricidad, son frágiles a la manipulación o son gases.
La principal característica que diferencia los metales de los no metales es la capacidad de conducir la electricidad.
Existen elementos que parecen metales, pero reaccionan como no metales. Estos elementos se conocen como metaloides y son el boro, el silicio, el germanio, el arsénico, el antimonio, el telurio y el polonio.
| Metales | No metales | |
|---|---|---|
| Definición | Son los elementos que tienen tendencia a perder electrones y a conducir la electricidad. | Son los elementos con tendencia a ganar electrones y malos conductores de la electricidad. |
| Características |
|
|
| Ejemplos |
|
|
De los 118 elementos en la tabla periódica, los metales representan el 80 % de los elementos. A continuación te presentamos los elementos de la tabla periódica y su correspondiente clasificación como metales, no metales y metaloides:
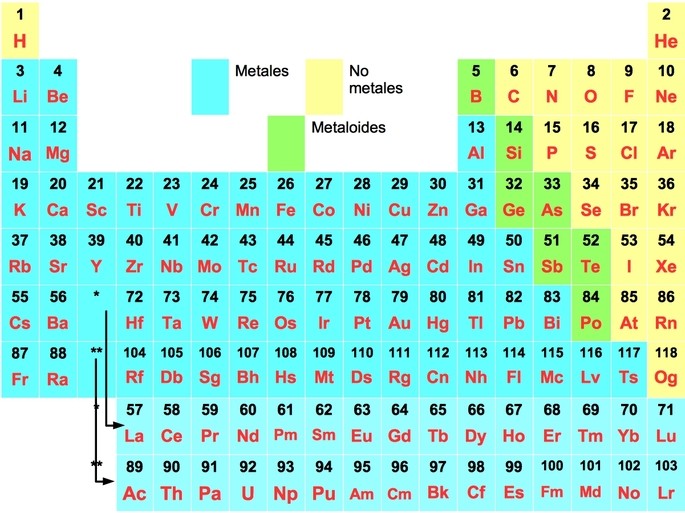
Qué son metales
Los elementos metálicos son aquellos que tienen tendencia a ceder electrones y pueden conducir la electricidad. Además, presentan un brillo característico, son maleables y dúctiles.
Están localizados en la parte izquierda de la tabla periódica, siendo los elementos más a la izquierda los que tienen carácter más metálico.
Los metales se pueden clasificar en:
- Los metales alcalinos son los elementos litio, sodio, potasio, rubidio, cesio y francio.
- Los metales alcalino-térreos son los elementos berilio, magnesio, calcio, estroncio, bario, y radio.
- Los metales de transición son los que se encuentran en el bloque central de la tabla periódica, y en ellos están incluidos el cobre, el oro, la plata, el platino, entre otros más.
Características de los metales
- Conducen la electricidad: permiten el movimiento de los electrones a través del material.
- Sus electrones de valencia se mueven libremente: los electrones de la capa más externa de los metales se pueden mover libremente.
- Son propensos a perder electrones: cuando los metales reaccionan, por lo general, pierden electrones.
- Son reactivos: la reactividad química de los metales aumenta bajando en el grupo, pero disminuye a lo largo del periodo.
- Se unen por enlaces metálicos: los metales establecen entre sí enlaces metálicos, un mar de electrones que se "pasean" entre los núcleos de los átomos.
- Son sólidos a temperatura ambiente: la mayoría de los metales son sólidos, a excepción del mercurio Hg, el galio y el cesio que son líquido a temperatura ambiente.
Ejemplos de metales
Aluminio
Es el metal más abundante de la corteza terrestre con brillo blanco-plateado, ligero, cuyo número atómico es 13. Es un sólido que se funde a los 660 °C. El aluminio se extrae de la bauxita, forma de óxido de aluminio hidratado.
Se usa ampliamente en utensilios de cocina y aplicaciones industriales por su elevada resistencia a la corrosión.

Bario
Es un metal de número atómico 56, perteneciente a los metales alcalino-térreos. Es un sólido que se funde a los 727 ºC, descubierto en 1808 por Humphrey Davy. Se obtiene de la barita, una sal de sulfato de bario.
El bario en forma pura tiene aspecto plateado como el plomo.
Berilio
Es el cuarto elemento de la tabla periódica, perteneciente a los metales alcalino-térreos. Es un sólido que se funde a 1287 ºC y se encuentra en la composición de las esmeraldas y las aguamarinas.

Bismuto
Es un metal quebradizo, cristalino y blanco, con número atómico 83, confundido por mucho tiempo por estaño o plomo. Es el más diamagnético de los metales y con la menor capacidad de transmitir calor. Con el bismuto se hacen aleaciones para recubrir objetos que pueden dañarse a altas temperaturas, como equipos de detección de fuego o extintores.
Calcio
Es el quinto elemento metálico más abundante de la corteza terrestre. Tiene un color plateado, es sólido duro, con número atómico 20. Forma parte de los metales alcalino-térreos y es constituyente de importantes estructuras biológicas, como los huesos, los dientes y las conchas.
Cesio
Es el metal más electropositivo y más alcalino. Se encuentra en estado líquido a temperatura ambiente, junto con el galio y el mercurio. El cesio explota al contacto con el agua y tiene una gran afinidad por el oxígeno. Se usa en los relojes atómicos.
Cromo
Es uno de los metales de transición, con número atómico 24, sólido que se funde a 2671 ºC. Se usa cromo para endurecer el acero, darle una superficie dura y brillante para prevenir la corrosión y en la fabricación de vidrio para darle el color verde.
Cobre
Es uno de los metales más importantes para el ser humano, que lo ha utilizado desde hace más de 5000 años. Su brillo rojizo metálico resalta además de ser maleable y dúctil, lo que permite su utilización en la construcción de joyería, utensilios de cocina y suministros eléctricos.

Hierro
Es el metal más común en la Tierra, ya que forma gran parte del núcleo del planeta. Su número atómico es 26, es duro, quebradizo, sólido que se funde a 1538 ºC. El hierro forma parte de los sistemas de transporte de oxígeno en los seres vivos. En su estado puro, el hierro es muy reactivo y se corroe rápidamente en ambientes húmedos.
Oro
Es el metal más maleable y dúctil, de gran belleza en estado puro. Su número atómico es el 79 y pertenece a los metales de transición. Es un buen conductor de la electricidad y el calor y resistente a la corrosión. Se usó como moneda y ahora es el estándar en el sistema monetario de muchos países.

Qué son no metales
Los elementos no metálicos son todos aquellos elementos que no encajan en las características de los metales. Dentro de los no metales encontramos los halógenos, los gases nobles, el hidrógeno, el carbono, nitrógeno, fósforo, el oxígeno, el azufre y el selenio.
Se localizan en la parte derecha de la tabla periódica, separados de los metales por los metaloides.
Características de los no metales
- No conducen la electricidad: los elementos no metálicos son malos conductores de la electricidad.
- Sus electrones de valencia están restringidos: los electrones de los no metales están más restringidos en su movimiento.
- Son propensos a ganar electrones: los átomos de elementos no metálicos cuando reaccionan tienden a aceptar electrones de otros elementos.
- Tienen reactividad: la reactividad química de los no metales disminuye en el grupo, pero aumenta en el período.
- Forman enlaces covalentes con otros no metales: los elementos no metálicos tienden a compartir sus electrones en la capa de valencia con otros no metales, formando enlaces covalentes.
Te puede interesar ver también Tipos de enlaces químicos
Ejemplos de no metales
Bromo
Es el único elemento no metal que se encuentra como un líquido marrón rojizo a temperatura ambiente. Su número atómico es 35 y pertenece al grupo de los halógenos. Se usa para hacer agentes a prueba de fuego, purificadores de agua, colorantes, medicinas y desinfectantes.
Carbono
Es el elemento no metálico con la mayor capacidad para combinarse con otros elementos, clave de la construcción de moléculas biológicas. Se encuentra libre en la naturaleza como diamante y grafito. En la atmósfera se encuentra combinado con el oxígeno como dióxido de carbono.

Te puede interesar ver también Ejemplos de compuestos orgánicos e inorgánicos.
Cloro
Es un gas amarillo-verdoso, con número atómico 17, perteneciente al grupo de los halógenos. Se encuentra en la naturaleza combinado con otros elementos, como la sal común NaCl. Los compuestos de cloro son ampliamente usados en el mundo entero, como desinfectantes, blanqueadores, purificación de agua, entre otros.
Flúor
Es el elemento más electronegativo y reactivo, pertenece al grupo de los halógenos, con número atómico 9. Es un gas corrosivo amarillo pálido en estado puro.
Helio
Es el segundo elemento de la tabla periódica y primero del grupo de los gases nobles. Su nombre se deriva del griego helios que significa "sol", donde fue identificado por primera vez en 1868. Junto con el hidrógeno es el elemento más abundante en todo el Universo.
Te puede interesar ver también:
Referencias
Lide, D. R. (editor) (2005). CRC Handbook of chemistry and physics, CRC Press, Boca Raton, Florida.
Vernon, R.E. (2013). Which elements are metalloids? Journal of Chemical Education 90:1703